Là Gì Nhỉ – Thế Nào Mới Là Electron Hóa Trị?
Bạn có bao giờ tự hỏi về Electron hóa trị và cách xác định số electron hóa trị không? Trong lĩnh vực hoá học, kiến thức về Electron hóa trị là vô cùng quan trọng và không thể phớt lờ. Vậy thì Electron hóa trị thực sự là gì? Làm sao để xác định chính xác số lượng electron hóa trị? Hãy cùng khám phá thông qua bài viết dưới đây tại Laginhi.com để hiểu rõ hơn về chủ đề này.
Bạn đang xem: Electron hóa trị là gì? Cách xác định số electron hóa trị
Electron hóa trị là gì?
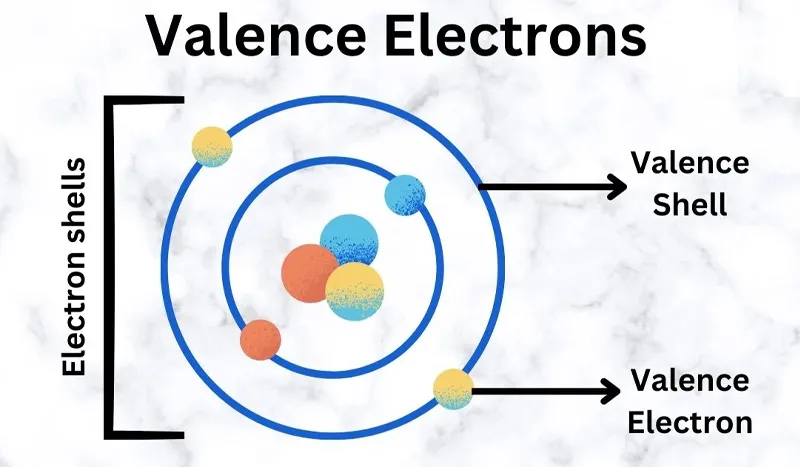
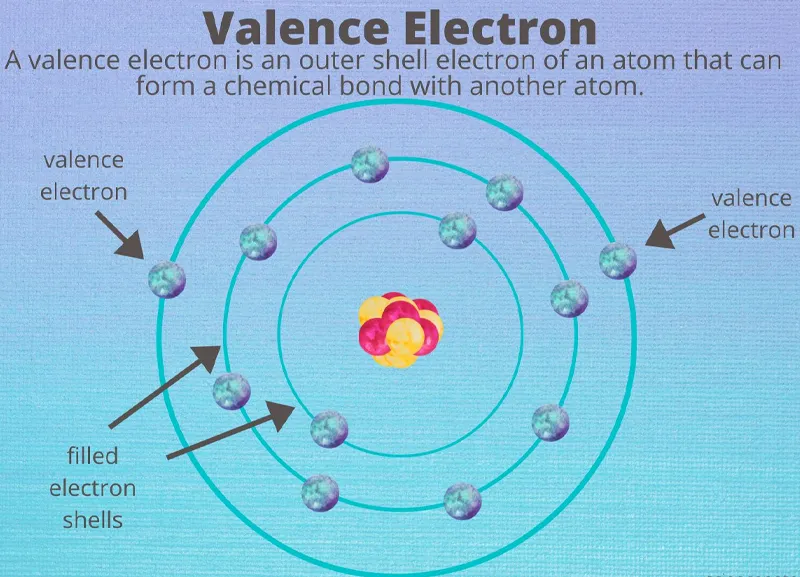
Electron hóa trị, hay còn gọi là electron ngoài cùng trong lĩnh vực vật lý và hóa học, là các electron đặt tại lớp vỏ bên ngoài của nguyên tử. Các electron hóa trị có thể tham gia hoặc không vào việc tạo liên kết hóa học, phụ thuộc vào trạng thái hóa học của nguyên tử đó. Khi tham gia tạo liên kết, chúng được gọi là electron liên kết.
Chúng ta có thể đánh giá tính chất hóa học của một nguyên tố thông qua việc quan sát electron hóa trị của nó. Chẳng hạn, có thể xác định được hóa trị của nguyên tố đó và khả năng liên kết với các nguyên tố khác, cũng như cách mà việc liên kết diễn ra. Cấu trúc electron của một nguyên tố sẽ ảnh hưởng đến khả năng phản ứng hóa học của chính nó.
Với các nguyên tố trong nhóm chính, electron hóa trị thường đặt ở lớp vỏ ngoài cùng của nguyên tử. Trong khi đó, đối với kim loại chuyển tiếp, electron hóa trị tập trung ở lớp vỏ bên trong.
Ví dụ 1:
Nguyên tử Natri (Na) có cấu hình electron là 1s² 2s² 2p⁶ 3s¹
- Lớp ngoài cùng: 3s¹
- Số electron hóa trị: 1
Trong lớp ngoài cùng, có 1 electron trong orbital 3s, vì vậy số electron hóa trị của nguyên tử natri là 1.
Ví dụ 2:
Nguyên tử Lưu huỳnh (S) có cấu hình electron là 1s² 2s² 2p⁶ 3s² 3p⁴
- Lớp ngoài cùng: 3s² 3p⁴
- Số electron hóa trị: 6
Trong lớp ngoài cùng, có 6 electron trong các orbital 3s và 3p, do đó số electron hóa trị của nguyên tử lưu huỳnh là 6.
Electron hoá trị và ứng dụng trong hóa học
Electron hoá trị đóng vai trò quan trọng trong các phản ứng hóa học do chúng có năng lượng cao hơn so với electron ở trong lớp năng lượng bên trong. Số lượng electron hoá trị không chỉ giúp xác định các tính chất hóa học của một nguyên tố, bao gồm hóa trị và khả năng tạo liên kết với các nguyên tố khác.
Xem thêm : Waifu, Husbando là gì? Top những Waifu trong anime được yêu thích nhất
Thông qua electron hoá trị, chúng ta có thể biết được nguyên tử nào có khả năng tạo liên kết dễ dàng, số lượng nguyên tử tham gia vào quá trình này, cũng như số lượng electron không ghép cặp.
Đặc Điểm Của Electron Hóa Trị
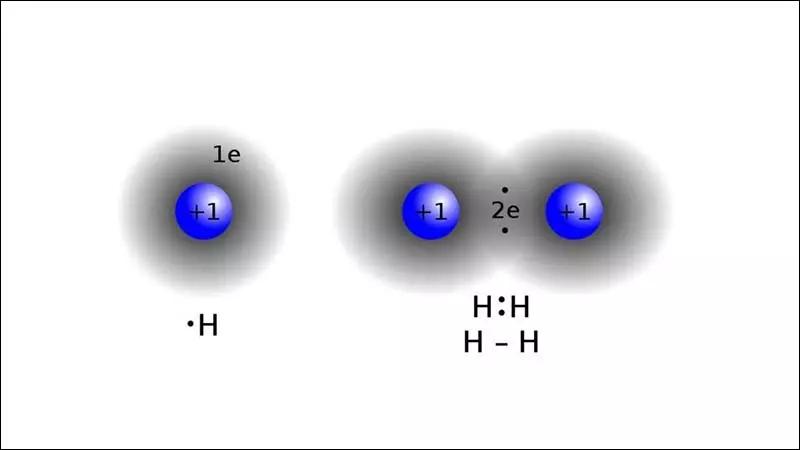
Electron hóa trị tương ứng với việc các electron nằm ở lớp ngoài cùng trong cấu trúc electron của một nguyên tử. Việc này quan trọng trong quá trình hình thành liên kết giữa các nguyên tử để tạo ra các hợp chất. Dưới đây là một số đặc điểm chính về electron hóa trị:
- Electron hóa trị ở các nguyên tố trong nhóm chính thường chỉ có mặt ở lớp electron bên ngoài.
- Ở các kim loại chuyển tiếp, electron hóa trị có thể tồn tại ở lớp electron trong.
- Một nguyên tử với một lớp electron ngoài cùng kín sẽ thường phản ánh tính chất hóa học của nó.
- Electron hóa trị có khả năng hấp thụ hoặc phát ra năng lượng dưới dạng photon.
- Chức năng chính của electron hóa trị là xác định khả năng dẫn điện của một nguyên tố, có thể là kim loại, phi kim hoặc bán kim.
### Cách Xác Định Electron Hóa Trị
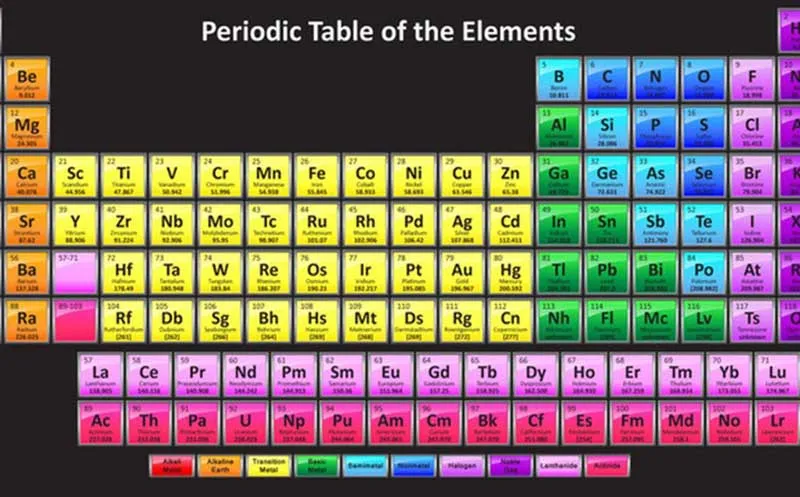
Xác định số electron hóa trị lớp ngoài cùng của một nguyên tố hóa học là một kỹ năng cần thiết. Dựa vào đó, có thể biết số liên kết trong phân tử, cơ sở của việc phân tử đó hình thành liên kết đôi chứ không phải liên kết đơn. Dựa vào bảng hệ thống tuần hoàn các nguyên tố hóa học là cách đơn giản để xác định số electron hóa trị của nguyên tố.
Bảng hệ thống tuần hoàn của Men-đê-lê-ép được chia làm 18 cột gọi là các nhóm. Ta có nhóm IA, IIA, IIIA,… hay IB, IIB, IIIB,… Số electron hóa trị của một nguyên tố trùng với số thứ tự của nhóm. Các nguyên tố thuộc cùng một cột thì có cùng electron hóa trị.
Các nguyên tố thuộc nhóm A thì số electron hóa trị là số electron lớp ngoài cùng của nguyên tố. Các nguyên tố thuộc nhóm B thì số electron hóa trị có thể nằm ở phân lớp ngoài cùng hoặc sát phân lớp ngoài cùng (nếu phân lớp này chưa bão hòa) của nguyên tố. Cụ thể:
- Các nguyên tố thuộc nhóm IA có 1 electron hóa trị
- Các nguyên tố thuộc nhóm IIA có 2 electron hóa trị
- Các nguyên tố thuộc nhóm IIIA có 3 electron hóa trị
- Các nguyên tố thuộc nhóm IVA có 4 electron hóa trị
- Các nguyên tố thuộc nhóm VA có 5 electron hóa trị
- Các nguyên tố thuộc nhóm VIA có 6 electron hóa trị
- Các nguyên tố thuộc nhóm VIIA có 7 electron hóa trị
- Các nguyên tố thuộc nhóm VIIIA có 8 electron hóa trị
Ví Dụ: Nguyên tử của Nitơ (N) và Photpho (P) đều nằm trong nhóm VA (15) nên có tối đa 5 electron hóa trị, cụ thể:
- Cấu trúc electron của Nitơ (N) là: 1s² 2s² 2p³. N có 5 electron hóa trị thuộc các orbital 2s² 2p³ của lớp ngoài cùng.
- Cấu trúc electron của Photpho (P) là: 1s² 2s² 2p⁶ 3s² 3p³. P có 5 electron hóa trị thuộc các orbital 3s² 3p³ của lớp ngoài cùng.
Bảng Hóa Trị
| Hóa Trị: 1 | Hóa Trị: 2 | Hóa Trị: 3 |
|---|---|---|
| Sodium Na+ | Magnesium Mg+2 | Aluminum Al+3 |
| Potassium K+ | Calcium Ca+2 | Iron (III) Fe+3 |
| Copper (I) Cu+ | Copper (II) Cu+2 | Nitride N-3 |
| Hydrogen H+ | Iron (II) Fe+2 | Phosphate PO4-3 |
| Hydride H- | Zinc Zn+2 | Gold (III) Au+3 |
| Chloride Cl- | Oxide O-2 | Titanium (III) Ti+3 |
| Bromide Br- | Sulphide S-2 | Ammonium Al+ |
| Carbonate CO2-2 | Hydroxide OH- | Sulphite SO3-2 |
| Nitrate NO3- | Sulphate SO4-2 | Oxalate CH3COO- |
Chúc bạn thành công trong việc xác định electron hóa trị của các nguyên tố hóa học!
Quy tắc hóa trị
Quy tắc hóa trị là tập hợp các nguyên tắc được sử dụng để xác định sự hóa trị của các nguyên tố trong các hợp chất hóa học. Quy tắc này biểu thị tích của chỉ số và hóa trị của một nguyên tố trong một hợp chất bằng sự tích của chỉ số và hóa trị của các nguyên tố khác trong hợp chất đó.
Ví dụ dưới đây sẽ giúp bạn hiểu rõ hơn về quy tắc hóa trị. Giả sử có hai nguyên tố A với hóa trị a và nguyên tố B với hóa trị b. Quy tắc hóa trị yêu cầu rằng tích của chỉ số và hóa trị a phải bằng tích của chỉ số và hóa trị b.
Công thức tổng quát như sau:
Xem thêm : Hanbok Hàn Quốc là gì? Ra đời khi nào, có các loại nào và ý nghĩa của Hanbok
aA + bB → AB
Trong công thức trên, a và b đại diện cho hóa trị của nguyên tố A và B. Khi nhân chỉ số và hóa trị của mỗi nguyên tố A và B trong phản ứng, tổng của chúng phải bằng nhau. Điều này cho thấy rằng tổng điện tích dương từ nguyên tố A và tổng điện tích âm từ nguyên tố B trong hợp chất AB là cân bằng.
Ví dụ: để tạo thành muối natri clorua (NaCl), nguyên tố natri (Na) có hóa trị +1 và nguyên tố clo (Cl) có hóa trị -1. Theo quy tắc hóa trị, chúng ta có:
(+1)Na + (-1)Cl → NaCl
Tích của chỉ số (+1) và hóa trị (+1) của natri bằng tích của chỉ số (-1) và hóa trị (-1) của clo, điều này đảm bảo rằng tổng điện tích của muối NaCl không có tổng điện tích dương hoặc âm.

Trong chương trình hóa học, kiến thức về Electron hóa trị đóng vai trò quan trọng và cần thiết cho mọi người hiểu biết. Vậy Electron hóa trị là gì? Làm thế nào để xác định số Electron hóa trị? Hãy cùng khám phá thông qua bài viết dưới đây.
Câu hỏi thường gặp
Electron hóa trị là gì?
Electron hóa trị, hay electron ngoài cùng, là các electron tại lớp electron vỏ ngoài cùng của nguyên tử. Chúng có thể tham gia hoặc không tham gia vào việc hình thành liên kết hóa học, phụ thuộc vào trạng thái hóa học của nguyên tử. Khi tham gia vào việc hình thành liên kết, chúng gọi là electron liên kết.
Electron hoá trị dùng làm gì?
Các electron hóa trị đóng vai trò quan trọng trong các phản ứng hóa học bởi vì chúng có năng lượng cao hơn so với electron ở bên trong. Số lượng electron hóa trị giúp xác định các tính chất hóa học của nguyên tố, bao gồm khả năng liên kết với các nguyên tố khác và quá trình hình thành liên kết.
Đặc điểm của electron hóa trị
Electron hóa trị nằm ở lớp vỏ ngoại cùng của cấu trúc electron của nguyên tử và đóng vai trò quan trọng trong việc tạo liên kết giữa các nguyên tử. Một số đặc điểm chính của electron hóa trị bao gồm việc tồn tại ở lớp electron vỏ ngoài cùng đối với nguyên tố nhóm chính và lớp vỏ bên trong đối với kim loại chuyển tiếp.
Cách xác định electron hóa trị
Để xác định số electron hóa trị của một nguyên tố, bạn có thể sử dụng bảng hệ thống tuần hoàn các nguyên tố hóa học. Số electron hóa trị của một nguyên tố tương đương với số thứ tự của nhóm mà nguyên tố đó thuộc vào trong bảng hệ thống tuần hoàn.
Quy tắc hóa trị
Quy tắc hóa trị là các nguyên tắc sử dụng để xác định hóa trị của các nguyên tố trong hợp chất hóa học. Quy tắc này giúp đảm bảo cân bằng điện tích dương và điện tích âm trong hợp chất.
Lưu ý về electron hóa trị
- Số electron hóa trị không giống hoá trị của nguyên tử.
- Hóa trị chỉ biểu thị khả năng tạo liên kết hóa học của nguyên tố trong từng phân tử hoặc hợp chất.
- Không thể xác định hóa trị chỉ dựa trên bảng tuần hoàn hóa học.
Tóm tắt
Trên đây là một tổng quan về Electron hóa trị và cách xác định chúng trong hóa học. Hi vọng rằng thông tin này sẽ giúp bạn hiểu rõ hơn về chủ đề này. Để biết thêm thông tin chi tiết, hãy truy cập trang web của chúng tôi.
Nguồn: https://laginhi.com
Danh mục: News