Đã bao giờ bạn tự hỏi về bí mật ẩn sau hiện tượng Phản Ứng Oxi Hóa Khử chưa? Tại sao nó lại mang tới những kết quả đặc biệt như vậy? Với sự hiểu biết sâu sắc về lĩnh vực này, Laginhi.com sẽ cùng bạn khám phá và giải đáp tất cả những thắc mắc qua bài viết dưới đây!
Phản ứng oxi hóa khử là gì?
Phản ứng oxi hóa khử là một quá trình quan trọng trong hóa học, xảy ra khi chất bị trao đổi electron. Phản ứng oxi hóa xảy ra khi một chất mất electron, còn phản ứng khử xảy ra khi một chất nhận electron. Điều này dẫn đến sự thay đổi về trạng thái oxi hóa của chất tham gia.
Bạn đang xem: Phản ứng oxi hóa khử là gì? Lý thuyết và bài tập về phản ứng oxi hóa khử
Trong cuộc sống hàng ngày, phản ứng oxi hóa khử đóng vai trò quan trọng trong nhiều quá trình, từ quá trình hô hấp của cơ thể đến việc sản xuất điện trong pin. Bằng cách hiểu rõ về cơ chế và ứng dụng của phản ứng oxi hóa khử, bạn sẽ có cái nhìn sâu hơn về cách mà thế giới xung quanh chúng ta hoạt động.
3: Các Phản Ứng Oxi Hóa Khử
Trong hóa học, các phản ứng oxi hóa khử đóng vai trò quan trọng trong việc chuyển đổi chất từ dạng này sang dạng khác. Ví dụ, khi một chất trao đổi electron với chất khác, đó được gọi là phản ứng oxi hóa khử. Quy trình này là cơ sở của nhiều hiện tượng hóa học và sinh học quan trọng. Để hiểu rõ hơn về các phản ứng này, hãy xem xét ví dụ sau.
Phản Ứng Oxi Hóa Khử:
- Ví dụ 1: Sự oxi hóa của sắt: Fe → Fe2O3
- Ví dụ 2: Sự khử tạo ra hidro: 2H2O → 2H2 + O2
Các phản ứng này thường xảy ra theo cặp, mỗi phản ứng oxi hóa đều đi kèm với một phản ứng khử tương ứng. Việc nắm vững cơ chế của các phản ứng oxi hóa khử sẽ giúp bạn hiểu rõ hơn về sự tương tác của các chất và quy luật tồn tại trong thế giới hóa học.Trong hóa học, các phản ứng oxi hóa – khử đóng một vai trò quan trọng trong việc chuyển đổi các chất từ dạng này sang dạng khác. Có ba loại chính: phản ứng oxi hóa – khử thông thường, phản ứng oxi hóa – khử nội phân và phản ứng oxi hóa – khử tự nhiên. Để hiểu rõ hơn về chúng, bạn có thể truy cập tại: https://luatminhkhue.vn/phan-ung-oxi-hoa-khu-la-gi.aspx#1-phan-ung-oxi-hoa-khu-la-gi.
Cách lập phương trình hóa khử
Khi muốn lập phương trình hóa khử, bạn cần tuân thủ 3 bước chính. Đầu tiên, xác định phản ứng oxi-hoá và khử. Tiếp theo, viết và cân bằng phương trình ion hoặc phân tử tham gia trong quá trình. Cuối cùng, cân bằng số oxi-hoá của từng nguyên tử trong phản ứng.
Việc lập phương trình hóa khử không chỉ giúp bạn hiểu rõ hơn về quá trình hóa học mà còn giúp tăng cường kiến thức và kỹ năng của bạn. Hãy thực hành nhiều để nâng cao khả năng lập phương trình hiệu quả hơn.
Ý nghĩa của phản ứng oxi hóa khử
Một trong những quá trình quan trọng trong hóa học là phản ứng oxi hóa khử. Đây không chỉ là một khía cạnh cơ bản của ngành hóa học mà còn có ứng dụng rộng rãi trong đời sống hàng ngày và các lĩnh vực công nghệ khác. Phản ứng này chủ yếu liên quan đến việc chuyển đổi electron giữa các chất, góp phần quan trọng trong việc duy trì sự cân bằng hóa học. Điều này giúp tạo ra năng lượng, sản phẩm cần thiết và cả tác động đến môi trường xung quanh chúng ta.
Bạn cần biết về quá trình phản ứng oxi hóa khử
Khi tìm hiểu về phản ứng oxi hóa khử, quý vị sẽ hiểu rõ hơn về cách mà các chất có thể tương tác với nhau thông qua việc trao đổi electron. Điều này không chỉ giúp củng cố kiến thức hóa học mà còn giúp quý vị hiểu rõ hơn về những ứng dụng thực tế của phản ứng này trong cuộc sống hàng ngày, từ quá trình hô hấp tới quá trình sản xuất và xử lý các sản phẩm hóa học.
Đặc điểm chính của phản ứng oxi hóa khử
- Chuyển đổi electron giữa các chất
- Sản xuất năng lượng và sản phẩm quan trọng
- Ảnh hưởng đến môi trường và quá trình sống cần thiết của các hệ sinh học
Với ý nghĩa quan trọng và tác động sâu rộng của phản ứng oxi hóa khử, việc hiểu biết về quá trình này sẽ giúp quý vị có cái nhìn tổng quan và sâu sắc về một trong những quá trình cơ bản nhất trong hóa học và cuộc sống hàng ngày.
Ví dụ minh họa
Cung cấp ví dụ minh họa là cách hiệu quả để giải thích một vấn đề phức tạp một cách dễ hiểu. Khi bạn thấy một tình huống được minh họa bằng ví dụ cụ thể, bạn sẽ dễ dàng áp dụng kiến thức đó vào thực tế. Ví dụ minh họa giúp làm rõ ý tưởng và tạo ra sự kết nối giữa lý thuyết và thực tế, từ đó giúp bạn hiểu sâu hơn vấn đề đang được đề cập. Điều này cũng giúp tăng cường sự hấp dẫn và hiểu biết của bạn đối với chủ đề đó.
Với việc sử dụng ví dụ minh họa, bạn có thể thấy rằng khái niệm trừu tượng trở nên cụ thể hơn và dễ dàng tiếp cận hơn. Hãy tận dụng các ví dụ minh họa để bổ sung cho kiến thức của bạn và làm cho thông tin trở nên sinh động và thú vị hơn.
Định nghĩa phản ứng oxi hóa khử
- Chất khử là gì? Chất khử chính là chất nhường electron hay là chất có số oxi hóa tăng sau phản ứng. Chất khử còn được gọi là chất bị oxi hóa.
- Chất oxi hóa là gì? Chính là chất nhận electron hay là chất có số oxi hóa tăng sau phản ứng. Chất oxi hóa còn được gọi là chất bị khử.
- Sự khử là gì? Sự khử một chất (quá trình khử) nghĩa là làm cho chất đó nhận electron hay làm giảm số oxi hóa của chất đó.
- Sự oxi hóa là gì? Chính là quá trình oxi hóa một chất là làm cho chất đó nhường electron hay làm tăng số oxi hóa của chất đó.
Điều này đồng nghĩa với việc sự khử và sự oxi hóa diễn ra đồng thời trong một phản ứng oxi hóa-khử.
Phản ứng oxi hóa khử trong hóa hữu cơ là quá trình hóa học mà trong đó cả hai quá trình oxi hóa và khử xảy ra đồng thời. Nó là sự chuyển giao electron giữa các chất, thay đổi số oxi hóa của chúng.
Ví dụ: Ta cùng xem ví dụ phương trình oxi hóa khử hữu cơ sau:
(H2 + Cl2 → 2HCl)
Xem thêm : Công tắc thông minh là gì? Có đặc điểm gì nổi bật?
Hidro là chất khử vì số oxi hóa của Clo tăng từ 0 lên +1.
Clo là chất oxi hóa vì số oxi hóa giảm từ 0 xuống -1.
Quá trình khử: (Cl2 + 2e → 2Cl-)
Quá trình oxi hóa: (H2 → 2H+ + 2e-)
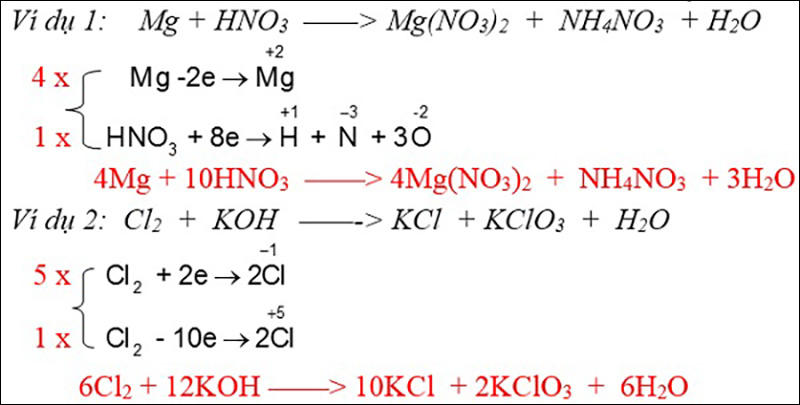
Số oxi hóa trong nguyên tử của phản ứng oxi hóa khử
Khi thảo luận về phản ứng oxi hóa khử, việc xác định số oxi hóa trên mỗi nguyên tử trong phân tử là không thể phủ nhận.
Có một số quy tắc hóa học quan trọng khi xác định số oxi hóa cụ thể:
- Số oxi hóa của đơn chất luôn là 0. Ví dụ: (overset{0}{Cu}); (overset{0}{Cl_{2}}); (overset{0}{S}),…
- Đối với ion, số oxi hóa bằng số điện tích của ion. Quy tắc này đúng cho cả ion tự do và ion trong các hợp chất. Ví dụ, ion (Cl^{-}) có số oxi hóa là -1.

Số oxi hóa trong hợp chất của phản ứng oxi hóa khử
Khi nghiên cứu các phản ứng oxi hóa khử, việc xác định số oxi hóa của các nguyên tố trong hợp chất là điều vô cùng quan trọng.
Trong hợp chất, oxi thường có số oxi hóa là -2, ngoại trừ trường hợp của peoxit và hợp chất flo.
Trái ngược với oxi, hidro thường có số oxi hóa bằng +1 trong hợp chất, trừ khi ở dạng hidrua.
Số oxi hóa của flo luôn là -1, và các kim loại nhóm IA, IIA, IIIA có số oxi hóa tương ứng là +1, +2 và +3.
Để dễ hiểu, tổng số oxi hóa của các nguyên tử trong phân tử phải luôn bằng 0. Ví dụ, trong axit nitric (HNO3), số oxi hóa của hidro là +1, trong khi nhóm nitrat (NO3-) có số oxi hóa là -1.

Phản ứng oxi hóa khử hữu cơ
Trong chương trình lớp 10, phản ứng oxi hóa-khử trở nên phong phú và sâu sắc hơn so với chương trình lớp 8. Ở cấp độ lớp 8, học sinh chỉ dừng lại ở việc định nghĩa cơ bản, nhưng khi bước vào lớp 10, bạn sẽ khám phá thêm về cách cân bằng phương trình phản ứng oxi hóa khử theo phương pháp thăng bằng electron. Để làm chủ phần bài tập về oxi hóa khử, hãy xem chi tiết trong sách giáo khoa Hóa học lớp 10.
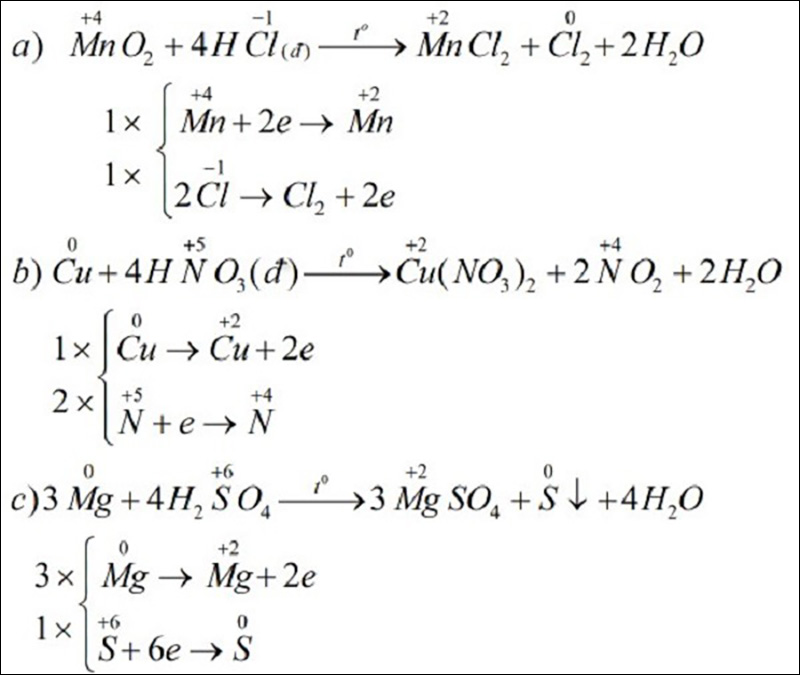
Cách Cân Bằng Phản Ứng Oxi Hóa Khử
Nguyên tắc chung: Để cân bằng phản ứng oxi hóa khử, bạn cần đảm bảo rằng số electron mà chất khử nhận được bằng số electron mà chất oxi hóa cho đi, hoặc số oxi hóa tăng của chất khử bằng số oxi hóa giảm của chất oxi hóa. Dưới đây là một số phương pháp cân bằng phản ứng oxi hóa khử phổ biến:
- Xác định số oxi hóa của từng chất tham gia trong phản ứng.
- Lập phương trình hóa học cho phản ứng oxi hóa khử.
- Cân bằng số oxi hóa tăng và giảm cho từng chất.
- Chỉnh sửa hệ số các chất trong phương trình để cân bằng số electron.
Bằng cách áp dụng các bước trên, bạn có thể hiểu rõ hơn về cách cân bằng các phản ứng oxi hóa khử một cách chính xác và hiệu quả.
Phương pháp nguyên tố nguyên tử
Khi thực hiện việc cân bằng, bạn cần chú ý viết các khí đơn chất (H2, O2, C12, N2…) dưới dạng nguyên tử riêng lẻ và áp dụng lập luận qua các bước cụ thể.
Ví dụ minh họa: Cân bằng phản ứng hóa học: P + O2 -> P2O5
Biểu diễn như sau: P + O -> P2O5
Xem thêm : Sữa dừa là gì? Lợi ích, công dụng của sữa dừa đối với sức khỏe
Để tạo thành một phân tử P2O5, bạn cần 2 nguyên tử P và 5 nguyên tử O:
2P + 5O -> P2O5
Đáng chú ý rằng phân tử oxi luôn bao gồm hai nguyên tử. Do đó, nếu sử dụng 5 phân tử oxi, số nguyên tử oxi sẽ tăng lên gấp đôi, khiến số nguyên tử P và số phân tử P2O5 cũng tăng lên theo cùng tỷ lệ, tức là 4 nguyên tử P và 2 phân tử P2O5.
Vì vậy: 4P + 5O2 -> 2P2O5
Phương pháp hóa trị tác dụng
Trong hóa học, phương pháp hóa trị tác dụng là cách chúng ta xác định hóa trị của các nguyên tử hoặc nguyên tử của các nguyên tố trong phân tử tham gia vào phản ứng hóa học và tạo thành phân tử mới. Để áp dụng phương pháp này một cách hiệu quả, chúng ta cần tuân theo các bước sau:
- Xác định hóa trị của các nguyên tử tham gia vào phản ứng
- Phân tích Bảng Số Chỉ và chia cho các hóa trị, từ đó chúng ta có thể xác định được các hệ số cần thiết cho phản ứng hóa học.
Phương pháp sử dụng hệ số phân số
Khi áp dụng phương pháp sử dụng hệ số phân số, việc gán hệ số vào các phương trình của các chất tham gia vào phản ứng không phân biệt giữa số nguyên và phân số, để đảm bảo rằng tổng số nguyên tử của mỗi nguyên tố ở cả hai bên bằng nhau. Tiếp theo, hãy rút gọn mẫu số chung của tất cả các hệ số.
Phương pháp “chẵn – lẻ”
Theo nguyên tắc của phương pháp này, sau khi cân bằng, số nguyên tử của một nguyên tố tại vế trái phải bằng số nguyên tử của cùng nguyên tố tại vế phải. Nếu số nguyên tử của một nguyên tố ở một vế là chẵn, thì số nguyên tử tương ứng ở vế kia cũng phải là số chẵn. Trong trường hợp số nguyên tử của một nguyên tố trong một công thức là lẻ, chúng ta cần nhân đôi số lượng đó để đạt được sự cân bằng.
Phương pháp xuất phát từ nguyên tố chung nhất
Một chiến lược quan trọng trong hóa học là lựa chọn nguyên tố xuất hiện trong nhiều hợp chất nhất khi thực hiện phản ứng để bắt đầu điều chỉnh tỷ lệ số lượng phân tử tham gia.
Phương Pháp Cân Bằng Electron
Kỹ thuật cân bằng electron đưa ra phương pháp cụ thể để cân bằng phản ứng hóa học một cách hiệu quả. Quá trình này diễn ra thông qua ba bước quan trọng:
a. Xác định thay đổi trong số oxi hóa của các chất tham gia.
b. Thực hiện việc cân bằng electron để đạt được trạng thái ổn định của các nguyên tử.
c. Đặt các hệ số đã tìm được vào phản ứng và tính toán để xác định các hệ số còn lại, giúp đảm bảo sự cân bằng toàn diện của phản ứng.
Cân Bằng Đại Số Trong Phản Ứng Hóa Học
Phương pháp cân bằng đại số được sử dụng để xác định hệ số phân tử của các chất tham gia và sản phẩm sau phản ứng hóa học. Trong phương pháp này, chúng ta coi hệ số là các ẩn số được kí hiệu bằng các chữ cái a, b, c, d… Dựa vào sự tương quan giữa các nguyên tử của các nguyên tố theo định luật bảo toàn khối lượng, chúng ta lập ra một hệ phương trình bậc nhất với nhiều ẩn số. Bằng cách giải hệ phương trình này và chọn các nghiệm là các số nguyên dương nhỏ nhất, chúng ta có thể xác định được hệ số phân tử của các chất trong phản ứng hóa học.
Hy vọng qua bài viết này, bạn đã hiểu rõ về phản ứng oxi hóa khử trong hóa học hữu cơ cũng như cách nhận biết phản ứng oxi hóa và phản ứng khử. Bạn đã biết được quá trình oxi hóa và quá trình khử diễn ra như thế nào. Nếu bạn có bất kỳ thắc mắc nào về phản ứng oxi hóa khử, hãy để lại ý kiến dưới đây để chúng ta có thể trao đổi thêm nhé!
Phản ứng oxi hóa khử trong Hóa học: Ý nghĩa và Cách xác định
FAQs
-
Phản ứng oxi hóa khử là gì?
Phản ứng oxi hóa khử là một quá trình hóa học với sự chuyển electron giữa các chất, thay đổi số oxi hóa của chúng. -
Phản ứng oxi hóa khử hữu cơ khác với phản ứng oxi hóa khử không?
Phản ứng oxi hóa khử hữu cơ là loại phản ứng trong hữu cơ với sự diễn ra của quá trình oxi hóa và khử đồng thời. -
Vì sao phải lập phương trình hóa học cho phản ứng oxi hóa khử hữu cơ?
Lập phương trình giúp mô tả rõ quá trình chuyển đổi electron giữa các chất, đồng thời thể hiện thay đổi số oxi hóa. -
Ý nghĩa của phản ứng oxi hóa khử là gì?
Phản ứng này đóng vai trò quan trọng trong quá trình chuyển đổi và tái cấu trúc hóa học của các chất. -
Phản ứng oxi hóa khử tự nhiên xảy ra như thế nào?
Trong tự nhiên, các phản ứng oxi hóa khử xảy ra thông qua sự trao đổi electron giữa các chất hữu cơ. -
Làm thế nào để xác định số oxi hóa trong các nguyên tử của phản ứng oxi hóa khử hữu cơ?
Việc xác định số oxi hóa yêu cầu tuân theo các quy tắc hóa học chuẩn xác để định lượng chính xác số oxi hóa trên từng nguyên tử.
Summary
Trên hết, phản ứng oxi hóa khử là một khía cạnh quan trọng trong hóa học, nhấn mạnh về sự chuyển electron và thay đổi số oxi hóa của các chất. Việc tìm hiểu và lập phương trình cho phản ứng này giúp mô tả và hiểu rõ quá trình diễn ra. Để học sâu hơn về phản ứng oxi hóa khử hữu cơ, bạn có thể tham khảo thêm trong sách giáo khoa Hóa học lớp 10. Đừng ngần ngại đặt câu hỏi và chia sẻ ý kiến của bạn để trao đổi kiến thức thêm với chúng tôi!
Nếu bạn quan tâm đến phản ứng oxi hóa khử hữu cơ và muốn khám phá thêm về chúng, hãy truy cập trang web của chúng tôi ngay hôm nay!
Nguồn: https://laginhi.com
Danh mục: News
